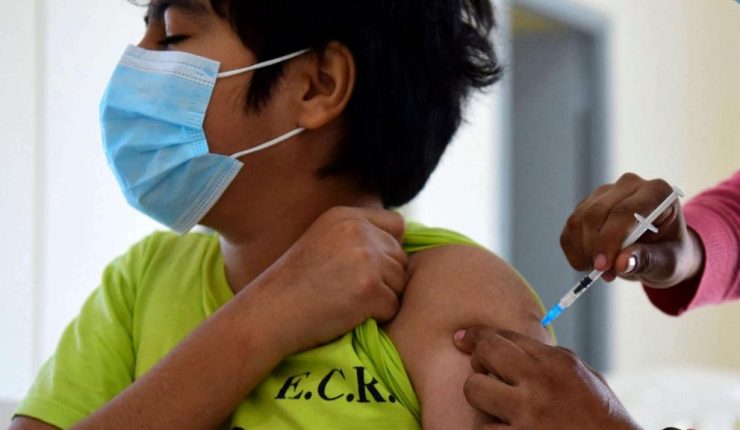
La farmacéutica publicó los primeros resultados para este grupo de edad tras un ensayo de fase 2/3 que incluyó a 2.268 participantes y donde se utilizó una dosis de 10 microgramos, menor que la de 30 microgramos que se ha utilizado para los mayores de 12 años.
En un anuncio muy esperado, Pfizer dijo el lunes que un ensayo de fase 2/3 mostró que su vacuna de COVID-19 era segura y generó una respuesta de anticuerpos “robusta” en niños de 5 a 11 años.
Estos son los primeros resultados de este tipo publicados para este grupo de edad para una vacuna de COVID-19 en EE. UU., y los datos aún no han sido revisados por pares ni publicados. Pfizer dijo que planea presentar pronto a la Administración de Medicamentos y Alimentos de EE.UU. (FDA) para una autorización de uso de emergencia (EUA).
El ensayo incluyó a 2.268 participantes de entre 5 y 11 años y utilizó un régimen de dos dosis de la vacuna administrada con 21 días de diferencia. Estos ensayos utilizaron una dosis de 10 microgramos, menor que la dosis de 30 microgramos que se ha utilizado para los mayores de 12 años.
“La dosis de 10 microgramos se seleccionó cuidadosamente como la dosis preferida por seguridad, tolerabilidad e inmunogenicidad en niños de 5 a 11 años”, dijo Pfizer en un comunicado de prensa.
Las respuestas inmunitarias de los participantes se midieron observando los niveles de anticuerpos neutralizantes en la sangre y comparando esos niveles con un grupo de control de personas de 16 a 25 años que recibieron un régimen de dos dosis con la dosis más grande de 30 microgramos.
Pfizer dijo que los niveles se comparan bien con los de las personas mayores que recibieron la dosis mayor, lo que demuestra una “fuerte respuesta inmunitaria en esta cohorte de niños un mes después de la segunda dosis”.
“Además, la vacuna de COVID-19 fue bien tolerada, con efectos secundarios generalmente comparables a los observados en participantes de 16 a 25 años“, dijo la compañía.
Un portavoz de Pfizer también confirmó que no hubo casos de miocarditis, un tipo de inflamación del corazón que se ha relacionado con las vacunas de ARNm.
Pfizer dijo que estos datos se incluirán en una “presentación a corto plazo” para EUA y que las empresas continuarán acumulando los datos necesarios para solicitar la aprobación de la FDA para personas de 5 a 11 años.
La vacuna de Pfizer / BioNTech está actualmente aprobada para personas de 16 años o más, y autorizada para su uso en personas de 12 a 15 años.
Pfizer dijo que espera datos de prueba para niños de tan solo 6 meses “tan pronto como el cuarto trimestre de este año”.
“Desde julio, los casos pediátricos de COVID-19 han aumentado en aproximadamente un 240% en EE.UU, lo que subraya la necesidad de vacunación de salud pública. Los resultados de estos ensayos proporcionan una base sólida para solicitar la autorización de nuestra vacuna para niños de 5 a 11 años, y planeamos enviarlos a la FDA y otros reguladores con urgencia”, dijo Albert Bourla, presidente y CEO de Pfizer, en el comunicado.
La Dra. Janet Woodcock, comisionada interina de la FDA, y el Dr. Peter Marks, director del Centro de Investigación y Evaluación Biológica de la FDA, dijeron en un comunicado este mes que la agencia revisaría los datos de una vacuna para niños más pequeños “lo más rápido posible, probablemente en cuestión de semanas en lugar de meses”, una vez que se presentó para su autorización.
“Sin embargo, la capacidad de la agencia para revisar estas presentaciones rápidamente dependerá en parte de la calidad y puntualidad de las presentaciones de los fabricantes”, escribieron.
Los pedidos de una vacuna de COVID-19 para niños más pequeños se han hecho más fuertes en los últimos meses a medida que aumentaban los casos entre los niños.
Las infecciones por coronavirus han aumentado “exponencialmente” entre los niños de Estados Unidos y ahora representan casi el 29% de todos los casos notificados en todo el país, informó la Academia Estadounidense de Pediatría la semana pasada.
Aún así, los funcionarios de salud de EE.UU. han enfatizado que los niños no son solo adultos pequeños, e incluso aquellos que se acercan a los 12 años no deben recibir la dosis de vacuna más grande disponible para las personas mayores.
“No queremos que los niños tengan efectos adversos. Por supuesto, queremos que puedan vacunarse lo más rápido posible, pero hagámoslo bien“, dijo Marks de la FDA en una charla junto a la chimenea organizada por ResearchAmerica Alliance la semana pasada.
“Aquí hay una diferencia porque no solo están recibiendo la misma dosis de la misma edad que una persona de 12 años o más. Tienen que recibir una dosis reducida. Y es por eso que no es una buena idea que los médicos tomen las cosas en sus propias manos en este momento“.